Mit der EU-Fälschungsschutzrichtlinie, verpflichtend seit Februar 2019, bilden Serialisierung und Erstöffnungsschutz das Fundament für fälschungssichere Arzneimittelpackungen. Jeder DataMatrix-Code enthält GTIN, Seriennummer, Charge und Verfallsdatum, was die Echtzeit-Prüfung via EMVS und securPharm ermöglicht. b+b Automations- und Steuerungstechnik warnt vor mangelhaften Datensätzen und präsentiert eine detaillierte Checkliste zum Druck-, Verifizierungs- und Datenmanagement. So lassen sich Chargen- und Verfallsdaten automatisch erfassen, Rückrufe effizient durchführen und Transparenz erhöhen. Scanstationen verbessern Datenerfassung und reduzieren Fehler.
Inhaltsverzeichnis: Das erwartet Sie in diesem Artikel
Falsified Medicines Directive stärkt europäische Arzneimittellieferkette seit Februar 2019

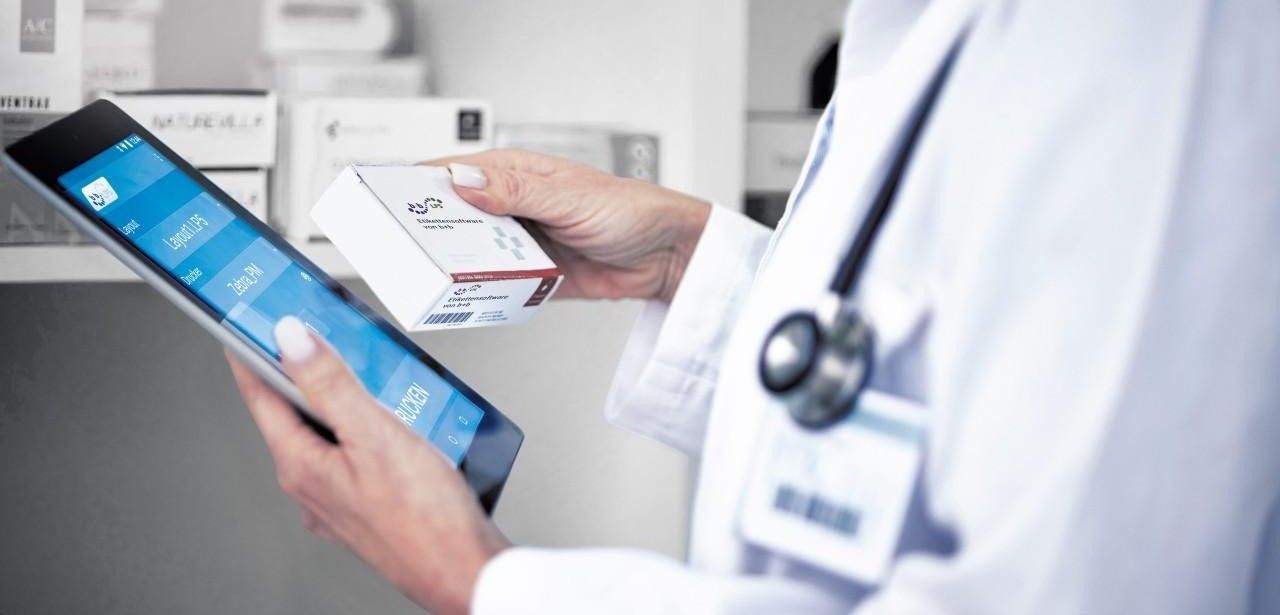
bb TE PV Pharmaserialisierung (Foto: b+b Automations- und Steuerungstechnik GmbH)
Abgeänderte Arzneimittelpräparate, die illegal nachgeahmt wurden, können nicht nur therapeutisch unwirksam sein, sondern können schwerwiegende Nebenwirkungen verursachen und das Vertrauen von Patienten in Gesundheitsdienste beschädigen. Um die Authentizität der regulären Lieferkette abzusichern, hat die EU im Jahr 2011 die Falsified Medicines Directive (FMD) initiiert, deren verbindliche Umsetzung seit Februar 2019 gilt. Dies umfasst verpflichtende Serialisierung jeder Packung, Datenübermittlung in zentrale Datenbanken und Erstöffnungsschutzmechanismen dauerhaft.
Jede Arzneimittelpackung erhält individuelle Seriennummer und Erstöffnungsschutz gegen Manipulation
Seriennummer und DataMatrix-Code bilden gemeinsam das Rückgrat der FMD-Sicherheitsarchitektur: Jede Packung erhält bei der Abfüllung eine einmalige Kennzeichnung, die maschinell auslesbar ist und alle relevanten Daten enthält. Der aufgeklebte 2D-Code speichert GTIN, individuelle Seriennummer, Charge sowie Verfallsdatum. Ein integrierter Erstöffnungsschutz am Karton macht jede offene Verpackung deutlich kenntlich. Dadurch können Logistikketten in Echtzeit überprüft und fehlerhafte Produkte rasch aussortiert werden. Dieses Verfahren minimiert Fälschungsrisiken und steigert Effizienz in Lager und Versand.
Individuelle Seriennummer und Verfallsdatum im DataMatrix-Code ermöglichen Rückverfolgung Packungen
Der 2D-DataMatrix-Code speichert definitiv den Produktcode (GTIN, NTIN oder PPN), eine individuelle Seriennummer, die Chargenkennung sowie das Verfallsdatum. Durch diese verpflichtende Kombination entsteht ein eindeutiger Datensatz für jede Packung, der während des gesamten Lieferwegs maschinenlesbar bleibt. Diese umfassende Kennzeichnung ermöglicht nicht nur die lückenlose Rückverfolgbarkeit, sondern unterstützt auch schnelle Authentifizierungs- und Rückrufprozesse, indem relevante Informationen sofort und ohne manuelle Eingabe verfügbar sind.
Warnmeldungen im Verifikationssystem durch mangelhafte Datenqualität können Prozesse stören
Das Unternehmen b+b Automations- und Steuerungstechnik GmbH hebt hervor, dass eine vernachlässigte Datenqualität in Serialisierungsprozessen gravierende Folgen haben kann. Fehlende oder inkorrekte Datensätze führen zu zahlreichen Warnhinweisen im Verifikationssystem, was Produktionslinien stoppt und Logistikaktionen verzögert. Um diese Risiken zu minimieren, empfiehlt b+b den Einsatz von Data-Governance-Richtlinien, automatisierten Validierungstools und Schulungsprogrammen für Mitarbeiter, damit Daten frühzeitig geprüft, Anomalien erkannt und Abläufe im gesamten Supply-Chain-Management zuverlässig optimiert werden. Regelmäßige Prozessreviews stärken Governance.
Hersteller liefern zentral an EMVS, sichern effektive Arzneimittelsicherheit europaweit
Über das European Medicines Verification System (EMVS) werden alle relevanten Serialisierungsdaten zentral erfasst und verwaltet. Hersteller senden die Codes inklusive GTIN, Seriennummer, Lot- und Verfallsinformationen an einen europäischen Hub. Nationale Systeme wie securPharm sind an dieses Netzwerk angebunden und führen bei der Abgabe in Apotheken oder Krankenhäusern Echtzeit-Abfragen durch. Auf diese Weise werden die Echtheit und Unversehrtheit jeder Arzneimittelpackung entlang der Lieferkette überprüft und dokumentiert. Dadurch werden Fälschungen zuverlässig verhindert.
Unvollständige Aggregationsdaten verhindern transparente Nachverfolgung täglich in der Lieferkette
Selbst nach korrekter Integration der Technik treten im Alltag schwerwiegende Prozessprobleme auf. Unklare Regeln beim Ausschleusen ermöglichen fehlerhafte Ausbuchungen oder Blockierungsfehler in der Supply-Chain. Decommissioning-Verfahren werden selten standardisiert umgesetzt, sodass abgemeldete Einheiten unbemerkt aktiviert bleiben. Die Abstimmung zwischen Druckausgabe, Verifikationsabfrage und Datenanlage funktioniert nicht durchgängig, wodurch Engpässe entstehen. Schließlich wird die Aggregationsdatenpflege nicht konsequent durchgeführt, was Transparenzdefizite und erhöhte Fehlerquoten in Logistik und Produktion nach sich zieht sowie Compliance-Risiken extern.
Umfassende Checkliste von b+b für effiziente Datenmanagement und EMVS-Integration
Die von b+b entwickelte Checkliste verfolgt einen ganzheitlichen Ansatz zur Risikooptimierung bei Serialisierungsprojekten. Sie umfasst detaillierte Beschreibungen für Druckprozesse inklusive Validierung der Druckqualität, standardisierte Verifizierungsprozeduren mit EMVS-Integration, strukturiertes Datenmanagement und die technische Anbindung an zentrale Verifikationsplattformen. Zusätzlich werden branchenspezifische Sonderprozesse wie Exportabwicklung, Retourenabgleich und Lohnverpackung erläutert. Damit erhalten Anwender einen umfassenden Leitfaden zur Einhaltung regulatorischer Anforderungen und effizienten Prozesssteuerung. Sie fördert Transparenz, Verantwortungsbewusstsein und nachhaltige Optimierung entlang der gesamten Lieferkette.
Transparente Seriennummern und Datenerfassung erhöhen Effizienz in Lagerung Vertrieb
Mittels präziser Serialisierung können Chargen- und Ablaufdaten nahtlos erfasst werden, wodurch manuelle Erfassungsfehler entfallen und die Datenintegrität erhöht wird. Echtzeit-Transparenz unterstützt zielgerichtete Rückrufaktionen und minimiert das Risiko gestörter Lieferprozesse. Detaillierte Datenauswertungen ermöglichen exakte Durchlaufzeit-Analysen für Produktions- und Logistikschritte. Ergänzend sorgen vertriebliche Kennzahlen auf Basis vollständiger Datensätze für eine smarte Optimierung von Distributionsstrecken und stärken das Gesamtergebnis durch verbesserte Effizienz Steigerung nachhaltiger Ressourcennutzung und reduzierte Betriebskosten resultieren aus übersichtlichen Prozessdaten sichtbar.
Pharma-Unternehmen setzen auf Serialisierung für lückenloses digitales effizientes Lieferketten-Monitoring
Mit dem flächendeckenden Einsatz digitaler Track-and-Trace-Systeme kann künftig jeder Produktschritt in der pharmazeutischen Lieferkette transparent erfasst werden. Eine lückenlose Dokumentation von Herstellung, Verpackung, Lagerung und Distribution schafft eine erweiterte Datenbasis, die die Serialisierung zum strategischen Eckpfeiler moderner Pharma-Logistik erhebt. Durch automatisierte Abgleiche mit Referenzdatenbanken wird Fälschungsschutz in Echtzeit gewährleistet, Ausgabefehler reduziert und Rückrufaktionen präzise eingeleitet. Gleichzeitig optimiert die fortwährende Datenanalyse interne Prozesse, verkürzt Lieferzeiten und verbessert Compliance. Mehr Sicherheit entsteht.
Hersteller und Lohnverpacker profitieren von regulatorischer Sicherheit und Digitalisierungsvorteilen
Durch die konsequente Anwendung der EU-FMD-Serialisierung werden Arzneimittelpackungen mit eindeutigen Identifikationsmerkmalen versehen, die eine effiziente Authentizitätsprüfung in Echtzeit ermöglichen. Registrierte Daten zu Seriennummer, Charge und Verfallsdatum verhindern Fälschungen und verbessern das Risikomanagement. Vollständig strukturierte Checklisten unterstützen reibungslose Abläufe und reduzieren Verzögerungen. Hersteller sowie Lohnhersteller nutzen die gewonnenen Transparenzdaten, um Prozesse zu optimieren, Rückrufe zu vereinfachen und nachhaltige Effizienzgewinne in der gesamten Pharma-Logistikkette unter Einbeziehung digitaler Monitoring- und Berichtssysteme zu realisieren.